Badan Pengawas Obat dan Makanan (BPOM) telah mengeluarkan Peraturan Badan Pengawas Obat dan Makanan No. 25 tahun 2023 tentang Kriteria dan Tata Laksana Registrasi Obat Bahan Alam. Peraturan ini mulai berlaku sejak 13 Oktober 2023. Beberapa ketentuan yang sebelumnya diatur dalam Peraturan Kepala BPOM No. HK.00.05.41.1384 tahun 2005 kini telah disesuaikan dengan PerBPOM 25/2023. Hal tersebut mencakup persyaratan keamanan, registrasi, dan izin edar untuk obat herbal.
Kepala BPOM RI, Dr. Ir. Penny Kusumastuti Lukito, MCP., mendukung pengembangan dan pemanfaatan jamu menjadi obat herbal terstandardisasi. Selain itu, Indonesia memiliki lebih dari 2.850 spesies tumbuhan obat dan 22.000 ramuan obat tradisional yang sudah teridentifikasi. Dengan keanekaragaman hayati yang melimpah, Indonesia memiliki peluang yang terbuka luas untuk mengembangkan dan memanfaatkan kekayaan obat herbal. Dukungan kebijakan tersebut membuat jamu sangat berpotensial untuk dikembangkan menjadi Obat Herbal Terstandardisasi (OHT) dan fitofarmaka.
Klasifikasi Ulang Obat Herbal: Ruang Lingkup dan Kriteria
Adapun perubahan yang terdapat didalam PerBPOM 25/2023 mencakup klasifikasi dan kriteria persyaratan keamanan untuk obat herbal. Pelaku usaha harus memenuhi kriteria yang dimaksud apabila ingin mendaftar dan mendapatkan izin edar.
Berikut perbandingan kategori obat herbal antara PerBPOM No.05/2005 dengan PerBPOM 25/2023:

Perlu dicatat bahwa PerBPOM 05/2005 tidak memberikan definisi khusus untuk obat-obatan herbal, hanya memberikan definisi tentang obat tradisional, termasuk jamu.
PerBPOM 25/2023 menetapkan bahwa khasiat obat herbal harus dibuktikan secara empiris, turun temurun, dan/atau ilmiah. Bukti empiris dapat bersumber dari naskah klasik, farmakope, monografi, atau referensi ilmiah lain yang diakui. Sementara itu, bukti ilmiah meliputi kegiatan ilmiah seperti uji praklinik dan/atau data klinik, serta referensi ilmiah yang diakui. Dalam kerangka baru ini, pelaku usaha obat herbal meliputi Usaha Mikro Obat Tradisional (UMOT), importir, dan badan usaha yang bergerak di bidang pemasaran obat herbal, selain Industri Obat Tradisional (IOT) dan Usaha Kecil Obat Tradisional (UKOT) yang diatur dalam PerBPOM 05/2005.
Prosedur Registrasi Wajib
PerBPOM 25/2023 memperkenalkan beberapa jenis registrasi baru untuk obat herbal, yaitu Registrasi dalam negeri (I, II, III, IV), Registrasi ekspor (V), dan Registrasi impor (VI). Masing-masing registrasi memerlukan dokumen yang harus diserahkan oleh pelaku usaha. Berikut adalah dokumen yang diperlukan untuk masing-masing jenis registrasi:

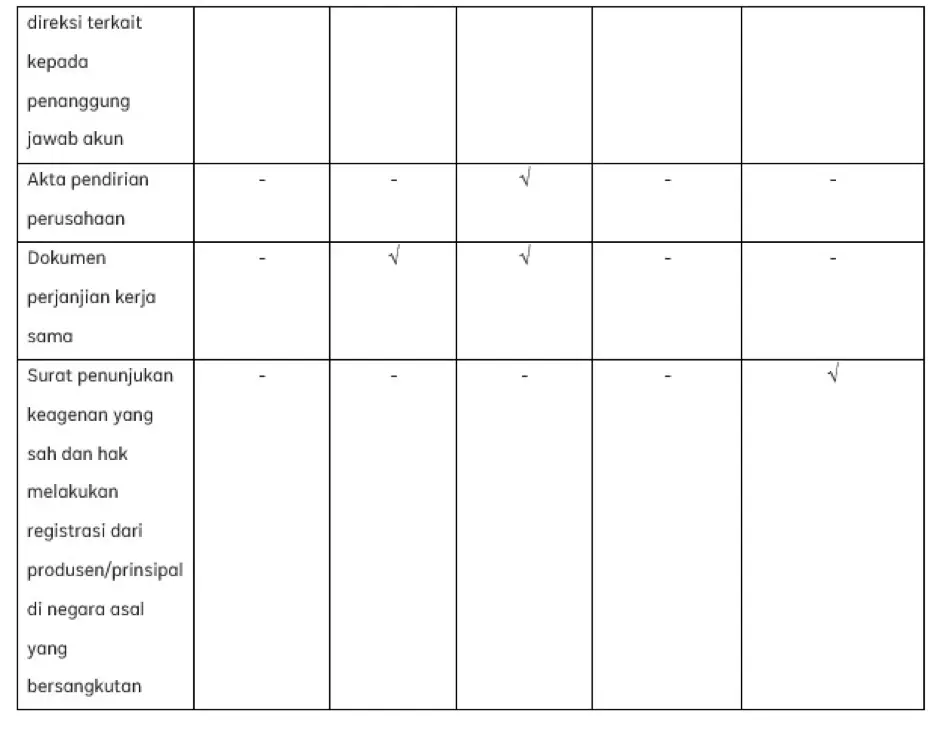
PerBPOM 25/2023 telah merevisi keseluruhan prosedur pengajuan permohonan registrasi obat herbal. Pelaku usaha harus mendaftarkan akun dan mengisi informasi yang diperlukan melalui website resmi BPOM atau secara offline jika terjadi keadaan kahar. Jika dianggap perlu oleh Kepala BPOM, mekanisme dengar pendapat akan dilakukan. Pelaku usaha harus menyampaikan permohonan registrasi (registrasi baru, registrasi variasi, atau registrasi ulang) beserta dokumen registrasi terkait.
Jika permohonan ditolak, pelaku usaha dapat mengajukan kembali permohonan dalam waktu tiga puluh hari setelah penolakan permohonan. Pelaku usaha yang mengajukan permohonan registrasi sebelum berlakunya PerBPOM 25/2023 akan tetap diproses permohonannya sesuai dengan PerBPOM 05/2005. Namun, pelaku usaha yang sebelumnya telah mendapatkan izin edar yang masih berlaku dan tidak memenuhi kriteria persyaratan keamanan yang ditentukan dalam PerBPOM 25/2023 akan diminta untuk menyesuaikan izinnya dengan kerangka baru dalam waktu dua tahun sejak diberlakukannya kerangka peraturan tersebut.
Sanksi Administratif yang Berlaku
Dalam PerBPOM 25/2023 terdapat sanksi administratif yang dapat diberlakukan bagi pelaku usaha obat herbal, yaitu berupa :
- Pembatalan/pencabutan nomor izin edar.
Pembatalan/pencabutan nomor izin edar dikenakan pada pelaku usaha yang tidak memproduksi atau mengimpor obat herbal selama dua tahun berturut-turut, tidak memproduksi atau mengimpor obat herbal dalam jangka waktu 1 (satu) tahun sejak izin edar diterbitkan, dan/atau sertifikat CPOTB dicabut.
- Pembekuan nomor izin edar.
- Penutupan akses daring pengajuan permohonan registrasi paling lama 1 (satu) tahun.
Disclaimer
Seluruh isi data dan informasi dalam Legal Brief ini merupakan kompilasi dari sumber-sumber terpercaya. Legal Brief ini tidak dimaksudkan dan tidak seharusnya dianggap sebagai nasihat atau opini hukum. Tidak disarankan mengambil tindakan berdasarkan informasi yang ada pada layanan ini tanpa mencari layanan profesional terlebih dahulu.
Dasar Hukum
- Peraturan No. 25 tahun 2023 tentang Kriteria dan Prosedur Registrasi Obat Herbal
Penutup
Jika Anda memiliki pertanyaan atau memerlukan lebih lanjut konsultasi mengenai legal brief ini, silakan menghubungi kami di :
- Timoty Ezra Simanjuntak, S.H., M.H. – Managing Partner – ezra@simanjuntaklaw.co.id
- Nico Ardianus Gultom, S.H. – Associate – office@simanjuntaklaw.co.id / info.simanjuntakandpartners@gmail.com





